रासायनिक अभिक्रियाएँ और समीकरण
Chemical Reactions and Equations Class Notes | NCERT Chapter 1 | Hindi + English
Chapter 1 – Class 10 NCERT Science
Story-format Notes | CBSE | State Boards | NEET | IIT-JEE Prep
Introduction- Chemical Reactions and Equations” Class 10 ka ek bahut important chapter hai jo Chemistry ki strong foundation banata hai. Isme hum samajhte hain ki daily life mein hone wale changes — jaise rusting, cooking, respiration — actually chemical reactions hote hain. In these notes, you will learn how to write and balance chemical equations in a simple and exam-friendly way. Content Hindi aur British English dono mein diya gaya hai taaki understanding clear ho aur answers properly likh pao. Isme story-based explanation, audio notes, NCERT book exercise solutions aur solved PDF bhi include hai. Yeh notes CBSE, State Boards, NEET aur IIT-JEE preparation ke liye useful hain aur quick revision mein bhi help karte hain.
Teacher: Om Sikarwar | CLASS ORB.COM
🎓 चार दोस्त और सर का विज्ञान का जादू
🏫 सुबह के 9 बज रहे थे। दिल्ली के एक स्कूल की Class 10 में Om Sikarwar Sir अभी-अभी
आए थे। उनके पीछे-पीछे चार पक्के दोस्त भी आए — Arjun (दिल्ली से), Priya (Chennai से),
Rohan (Lucknow से), और Sonu (Jaipur से)।
ये चारों हमेशा साथ बैठते, एक-दूसरे से पूछते और सर से जमकर सवाल करते।
Sir ने blackboard पर लिखा — ‘Chemical Reactions and Equations’
💬 Sir Om Sikarwar:
“बच्चों, पहले एक ज़रूरी सवाल — अगर मैं लोहे की कील को बाहर बरसात में छोड़ दूँ तो क्या होगा?”
💬 Arjun (उत्साह से):
“Sir, उस पर जंग लग जाएगी!”
💬 Sir:
“बिल्कुल सही, Arjun! और क्या कील वापस लोहा बन सकती है?”
“नहीं ना? — क्योंकि एक Chemical Reaction हो चुकी है। आज हम यही समझेंगे!”
Chemical Reaction क्या होती है? — इसे समझने के लिए Sir ने कुछ रोज़ाना की बातें पूछीं:
- दूध गर्मियों में खट्टा हो जाता है
- लोहे की चीज़ें बाहर छोड़ने से ज़ंग लग जाती है
- अंगूर किण्वित होकर वाइन बनता है
- खाना पकाया जाता है
- खाना हमारे शरीर में पचता है
- हम साँस लेते हैं
📌 KEY CONCEPT:
जब किसी पदार्थ का स्वभाव या पहचान बदल जाए — तो Chemical Reaction हुई।
इसे हम कैसे पहचानें? — नीचे पढ़ो!
▶ Chemical Reaction होने के संकेत (Signs of Chemical Reaction)
- रंग में बदलाव (Change in colour)
- गैस बनना (Evolution of gas)
- तापमान में बदलाव (Change in temperature)
- अवस्था में बदलाव (Change in state)
💬 Priya (सोचते हुए):
“Sir, जब मैं नींबू का रस चीनी में मिलाती हूँ — क्या वो chemical reaction है?”
💬 Sir:
“बहुत अच्छा सोचा Priya! नहीं — वो Physical Change है क्योंकि दोनों चीज़ें अलग की जा सकती हैं।”
“लेकिन अगर उसी नींबू के रस को रखकर छोड़ दो और वो किण्वित हो जाए — तो हाँ, Chemical Reaction!”
📝 1.1 रासायनिक समीकरण (Chemical Equations)
Rohan बोला — ‘Sir, जब भी कोई reaction होती है तो हम उसे कैसे लिखते हैं?’
Sir मुस्कुराए और बोले — ‘पहले शब्दों में लिखते हैं, फिर symbols में।’
▶ Word Equation (शब्द-समीकरण)
Magnesium ribbon जब हवा में जलती है तो —
Magnesium + Oxygen → Magnesium Oxide
यहाँ → का मतलब है: ‘बनता है’ या ‘अभिक्रिया होती है’
बायीं तरफ (LHS) = Reactants (अभिकारक) — जो चीज़ें reaction में शामिल होती हैं
दायीं तरफ (RHS) = Products (उत्पाद) — जो नई चीज़ बनती है
▶ Symbolic / Chemical Equation (रासायनिक समीकरण)
⚗️ Mg + O₂ → MgO
📌 यह एक Skeletal Chemical Equation है — यानी अभी balanced नहीं है।
इसे balance करना ज़रूरी है — क्योंकि atoms न बनते हैं, न नष्ट होते हैं।
💬 Sonu:
“Sir, balance करना क्यों ज़रूरी है? अगर न करें तो क्या होगा?”
💬 Sir:
“बहुत अच्छा सवाल Sonu! प्रकृति का एक नियम है — Law of Conservation of Mass।”
“जितना mass reaction से पहले हो, उतना ही बाद में होना चाहिए।”
“अगर हम equation balance नहीं करते तो हम इस नियम का उल्लंघन करते हैं।”
1.1.2 Balanced Chemical Equations — Balancing सीखें
Sir ने blackboard पर Fe + H₂O → Fe₃O₄ + H₂ लिखा और बोले:
‘चलो इसे step-by-step balance करते हैं — Rohan, हर element count करो!’
Step I — हर formula के चारों ओर box बनाओ:
⚗️ [Fe] + [H₂O] → [Fe₃O₄] + [H₂]
Step II — दोनों sides पर atoms गिनो:
|
Element |
LHS (Reactants) |
RHS (Products) |
|
Fe |
1 |
2 |
|
H |
2 |
2 |
|
O |
1 |
3 |
Step III — Oxygen सबसे ज़्यादा atoms वाला compound है (Fe₂O₃ में 3 O हैं)।
LHS पर O सिर्फ 1 है, RHS पर 3 है। तो H₂O के सामने 4 लगाओ:
⚗️ [Fe] + 4[H₂O] → [Fe₃O₄] + [H₂] (partly balanced)
Step IV — H balance करो। LHS पर 8H हैं, तो RHS पर 4H₂ रखो:
⚗️ [Fe] + 4[H₂O] → [Fe₃O₄] + 4[H₂] (partly balanced)
Step V — Fe balance करो। RHS पर 2 Fe हैं, तो LHS पर 3Fe रखो:
⚗️ 3[Fe] + 4[H₂O] → [Fe₂O₃] + 4[H₂]
Step VI — Check करो:
⚗️ 3Fe + 4H₂O → Fe₂O₃ + 4H₂ ✅ Balanced!
📌 Physical States लिखना:
(s) = solid | (l) = liquid | (g) = gas | (aq) = aqueous (पानी में घुला हुआ)
Final balanced equation with states:
3Fe(s) + 4H₂O(g) → Fe₂O₃(s) + 4H₂(g)
🔥 1.2 रासायनिक अभिक्रियाओं के प्रकार (Types of Chemical Reactions)
अब Sir ने कहा — ‘बच्चों, Chemistry में reactions कई तरह की होती हैं।’
‘हम एक-एक करके सबको story की तरह समझेंगे।’
Arjun बोला — ‘Sir, जैसे इंसान कई तरह के होते हैं, वैसे reactions भी?’
Sir हँसे — ‘बिल्कुल Arjun! बहुत अच्छी सोच है!’
1.2.1 संयोजन अभिक्रिया — Combination Reaction
💬 Sir:
“Priya, अगर दो अलग-अलग चीज़ें मिलकर एक नई चीज़ बनाएं — तो क्या होगा?”
💬 Priya:
“Sir, Combination होगी!”
💬 Sir:
“Exactly! जब दो या दो से अधिक पदार्थ मिलकर एक product बनाते हैं — Combination Reaction।”
उदाहरण 1 — Calcium oxide + Water → Slaked lime + Heat
⚗️ CaO(s) + H₂O(l) → Ca(OH)₂(aq) + Heat
यह reaction इतनी heat छोड़ती है कि beaker छूने पर बहुत गर्म लगता है।
Calcium hydroxide को slaked lime (बुझा हुआ चूना) कहते हैं।
Whitewashing (चूना-पोती) में यही Ca(OH)₂ use होता है।
उदाहरण 2 — Coal का जलना:
⚗️ C(s) + O₂(g) → CO₂(g)
उदाहरण 3 — पानी का बनना:
⚗️ 2H₂(g) + O₂(g) → 2H₂O(l)
📌 KEY CONCEPT — Exothermic Reaction:
जब reaction में heat बाहर निकलती है — उसे Exothermic Reaction कहते हैं।
Combination reactions अक्सर exothermic होती हैं।
अन्य Exothermic reactions:
- Natural gas का जलना: CH₄(g) + 2O₂(g) → CO₂(g) + 2H₂O(g)
- Respiration (श्वसन): C₆H₁₂O₆(aq) + 6O₂(aq) → 6CO₂(aq) + 6H₂O(l) + Energy
- Vegetable matter का compost बनना
1.2.2 वियोजन अभिक्रिया — Decomposition Reaction
Rohan ने पूछा — ‘Sir, अगर Combination reaction का उल्टा हो — तो क्या होगा?’
Sir बोले — ‘शाबाश Rohan! उल्टा यानी — एक पदार्थ टूटकर दो या ज़्यादा बन जाए।’
‘इसे Decomposition Reaction कहते हैं!’
जब एक reactant टूटकर दो या अधिक products बनाता है — Decomposition Reaction।
Types of Decomposition:
▶ (i) Thermal Decomposition — गर्मी से टूटना
उदाहरण — Ferrous Sulphate का heating से decomposition:
⚗️ 2FeSO₄(s) →[Heat] Fe₂O₃(s) + SO₂(g) + SO₃(g)
FeSO₄ crystals हरे रंग के होते हैं। Heating के बाद रंग बदलकर भूरा/लाल हो जाता है।
साथ ही जलते सल्फर की गंध आती है।
उदाहरण — Limestone का thermal decomposition:
⚗️ CaCO₃(s) →[Heat] CaO(s) + CO₂(g)
यह reaction cement industry में बहुत important है।
Calcium oxide को quicklime (कच्चा चूना) कहते हैं।
▶ (ii) Electrolytic Decomposition — बिजली से टूटना
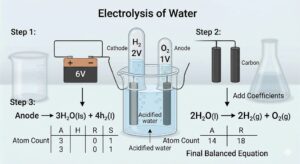
उदाहरण — पानी का electrolysis:
⚗️ 2H₂O(l) →[Electricity] 2H₂(g) + O₂(g)
Hydrogen gas (H₂) cathode पर जमा होती है — 2 volume
Oxygen gas (O₂) anode पर जमा होती है — 1 volume
इसीलिए H₂ का volume O₂ से double होता है।
▶ (iii) Photolytic Decomposition — प्रकाश से टूटना
उदाहरण — Silver chloride पर sunlight पड़ने से:
⚗️ 2AgCl(s) →[Sunlight] 2Ag(s) + Cl₂(g)
Silver bromide भी same तरह से react करती है:
⚗️ 2AgBr(s) →[Sunlight] 2Ag(s) + Br₂(g)
यही reactions Black & White Photography में use होती हैं।
📌 KEY CONCEPT — Endothermic Reaction:
जब reaction में heat अवशोषित (absorb) होती है — उसे Endothermic Reaction कहते हैं।
Decomposition reactions energy लेती हैं — heat, light या electricity के रूप में।
याद रखो: Combination ↔ Decomposition — ये एक-दूसरे के विपरीत हैं।
💬 Sonu:
“Sir, तो Black & White photos में जो image बनती है — वो silver की वजह से है?”
💬 Sir:
“हाँ Sonu! Silver nitrate की coating वाली film पर जब light पड़ती है तो silver बनता है।”
“जहाँ ज़्यादा light — वहाँ ज़्यादा silver — वहाँ ज़्यादा dark। यही photo बनती है!”
Photography में use होता है:
-
Silver chloride (AgCl)
-
Silver bromide (AgBr)
⚡ 1.2.3 विस्थापन अभिक्रिया — Displacement Reaction
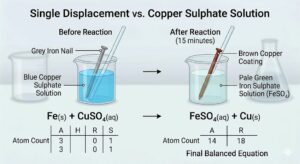
Arjun ने लोहे की कील copper sulphate में डालते देखा था।
उसने पूछा — ‘Sir, कील का रंग क्यों बदल गया? और solution हल्का क्यों पड़ा?’
Sir बोले — ‘यही है Displacement Reaction का जादू!’
जब एक अधिक reactive element, कम reactive element को उसके compound से निकाल दे —
उसे Displacement Reaction कहते हैं।
Activity 1.9 की reaction:
⚗️ Fe(s) + CuSO₄(aq) → FeSO₄(aq) + Cu(s)
Iron ने Copper को उसके compound CuSO₄ से निकाल दिया।
क्योंकि Iron, Copper से ज़्यादा reactive है।
नतीजा: Blue CuSO₄ solution का रंग हल्का पड़ गया — Cu जमा हुआ।
और उदाहरण:
⚗️ Zn(s) + CuSO₄(aq) → ZnSO₄(aq) + Cu(s)
⚗️ Pb(s) + CuCl₂(aq) → PbCl₂(aq) + Cu(s)
Zinc और Lead — दोनों Copper से ज़्यादा reactive हैं।
📌 IIT-JEE / NEET TIP:
Reactivity Series (Metals): K > Na > Ca > Mg > Al > Zn > Fe > Pb > Cu > Ag > Au
जो metal ऊपर है वो नीचे वाले को displace करती है।
This is the KEY concept for electrochemistry too!
1.2.4 द्विविस्थापन अभिक्रिया — Double Displacement Reaction
💬 Priya:
“Sir, अगर दो compounds के बीच ions की अदला-बदली हो तो?”
💬 Sir:
“तो Double Displacement Reaction होती है Priya!”
“दोनों compounds के ions आपस में exchange होते हैं।”
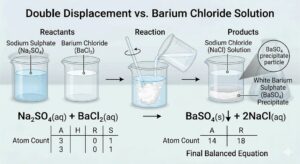
Activity 1.10 — Sodium sulphate + Barium chloride:
⚗️ Na₂SO₄(aq) + BaCl₂(aq) → BaSO₄(s) + 2NaCl(aq)
BaSO₄ एक white precipitate (सफेद अवक्षेप) बनता है जो पानी में नहीं घुलता।
ऐसी reactions जिनमें precipitate बने — Precipitation Reactions कहलाती हैं।
📌 Precipitation Reaction = Double Displacement Reaction जिसमें insoluble salt बने।
BaSO₄ का बनना SO₄²⁻ ions की presence test करने के लिए use होता है।
(NEET में यह concept बार-बार आता है!)
🔴🔵 1.2.5 ऑक्सीकरण और अपचयन — Oxidation & Reduction (Redox)
Rohan ने एक experiment देखा था — copper powder को गर्म करने पर वो काला पड़ गया।
उसने पूछा — ‘Sir, ऐसा क्यों हुआ?’
Sir बोले — ‘यही Oxidation है! Copper ने oxygen gain की!’
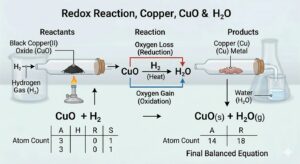
Activity 1.11 — Copper powder को गर्म करना:
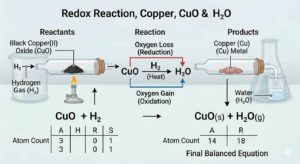
⚗️ 2Cu(s) + O₂(g) →[Heat] 2CuO(s)
Copper ने oxygen gain किया → Copper oxidised हुआ
Black CuO (copper(II) oxide) बना।
अब अगर उस CuO पर hydrogen gas गुज़ारें:
⚗️ CuO(s) + H₂(g) →[Heat] Cu(s) + H₂O(l)
CuO ने oxygen खोई → CuO reduced हुआ → फिर से भूरा copper बना
H₂ ने oxygen gain की → H₂ oxidised हुआ
📌 DEFINITIONS:
- Oxidation = Oxygen gain / Hydrogen loss
- Reduction = Oxygen loss / Hydrogen gain
- Oxidising Agent = वो जो oxygen देता है (खुद reduce होता है) = CuO
- Reducing Agent = वो जो oxygen लेता है (खुद oxidise होता है) = H₂
- Redox Reaction = जहाँ oxidation और reduction एक साथ हों
💬 Arjun (confused):
“Sir, यह थोड़ा उलझा हुआ है — जो खुद reduce हो वो दूसरे को oxidise करे?”
💬 Sir (मुस्कुराते हुए):
“Arjun, एक example सोचो। मान लो एक teacher जो हमेशा दूसरों को knowledge देता है।”
“उसका खुद का knowledge कम होता जाता है (reduce) लेकिन students gain करते हैं।”
“Oxidising agent भी ऐसा ही है — खुद lose करता है, दूसरे को gain कराता है।”
More Redox Examples:
⚗️ ZnO + C → Zn + CO [Carbon reduces ZnO, Carbon oxidised]
⚗️ MnO₂ + 4HCl → MnCl₂ + 2H₂O + Cl₂
🌍 1.3 रोज़मर्रा की ज़िंदगी में Oxidation के प्रभाव
Sonu घर से नई cycle लाया था। एक हफ्ते बाद उसने notice किया —
‘Sir! मेरी cycle पर जंग लग रही है!’
Sir बोले — ‘Sonu, यही Corrosion है। Chemistry अब तुम्हारे घर तक आ गई!’
▶ 1.3.1 संक्षारण — Corrosion
जब धातुएँ moisture, acid, oxygen की वजह से खराब होती हैं — corrosion।
- Iron पर जंग — reddish brown powder (Fe₂O₃.xH₂O)
- Silver पर काली परत — tarnishing
- Copper पर हरी परत — basic copper carbonate
Corrosion से नुकसान:
- Cars, bridges, ships, iron railings खराब होती हैं
- हर साल enormous amount of money खर्च होता है damaged iron को replace करने में
▶ 1.3.2 विकृतगंधिता — Rancidity
जब खाने में मौजूद fats और oils oxidise हो जाती हैं — Rancidity।
नतीजा: खाने की smell और taste बदल जाती है — बासी, खट्टी गंध आती है।
Rancidity रोकने के उपाय:
- Antioxidants मिलाना (जो oxidation को रोकें)
- Nitrogen gas से flush करके airtight containers में रखना
- Refrigerator में रखना
- Chips packets में Nitrogen gas भरना
📌 IIT-JEE / NEET CONNECTION:
Rancidity एक oxidation reaction है।
Antioxidants जैसे BHA (Butylated Hydroxyanisole) का use food preservation में।
यह concept Organic Chemistry तक जुड़ता है।
📊 Chapter Summary — Quick Revision Table
|
Type of Reaction |
Definition |
Example |
|
Combination |
2+ substances combine to form 1 product |
CaO + H₂O → Ca(OH)₂ |
|
Decomposition |
1 substance breaks into 2+ products |
2FeSO₄ → Fe₂O₃ + SO₂ + SO₃ |
|
Displacement |
More reactive metal displaces less reactive |
Fe + CuSO₄ → FeSO₄ + Cu |
|
Double Displacement |
Ions exchange between 2 compounds |
Na₂SO₄ + BaCl₂ → BaSO₄ + 2NaCl |
|
Oxidation |
Oxygen gain / Hydrogen loss |
2Cu + O₂ → 2CuO |
|
Reduction |
Oxygen loss / Hydrogen gain |
CuO + H₂ → Cu + H₂O |
|
Exothermic |
Heat released in reaction |
Combustion, Respiration |
|
Endothermic |
Heat absorbed in reaction |
Decomposition reactions |
|
Corrosion |
Metal surface deteriorates due to env. |
Rusting of iron |
|
Rancidity |
Oxidation of fats/oils = stale food |
Stale chips, butter |
⚗️ All Important Balanced Equations — Board + NEET + IIT-JEE
▶ Combination Reactions
⚗️ CaO(s) + H₂O(l) → Ca(OH)₂(aq) + Heat
⚗️ C(s) + O₂(g) → CO₂(g)
⚗️ 2H₂(g) + O₂(g) → 2H₂O(l)
⚗️ CO(g) + 2H₂(g) →[340°C, catalyst] CH₃OH(l)
⚗️ 6CO₂(aq) + 12H₂O(l) →[Sunlight, Chlorophyll] C₆H₁₂O₆(aq) + 6O₂(aq) + 6H₂O(l)
▶ Decomposition Reactions
⚗️ 2FeSO₄(s) →[Heat] Fe₂O₃(s) + SO₂(g) + SO₃(g)
⚗️ CaCO₃(s) →[Heat] CaO(s) + CO₂(g)
⚗️ 2Pb(NO₃)₂(s) →[Heat] 2PbO(s) + 4NO₂(g) + O₂(g)
⚗️ 2H₂O(l) →[Electricity] 2H₂(g) + O₂(g)
⚗️ 2AgCl(s) →[Sunlight] 2Ag(s) + Cl₂(g)
⚗️ 2AgBr(s) →[Sunlight] 2Ag(s) + Br₂(g)
▶ Displacement Reactions
⚗️ Fe(s) + CuSO₄(aq) → FeSO₄(aq) + Cu(s)
⚗️ Zn(s) + CuSO₄(aq) → ZnSO₄(aq) + Cu(s)
⚗️ Pb(s) + CuCl₂(aq) → PbCl₂(aq) + Cu(s)
▶ Double Displacement Reactions
⚗️ Na₂SO₄(aq) + BaCl₂(aq) → BaSO₄(s)↓ + 2NaCl(aq)
▶ Redox Reactions
⚗️ 2Cu(s) + O₂(g) →[Heat] 2CuO(s)
⚗️ CuO(s) + H₂(g) →[Heat] Cu(s) + H₂O(l)
⚗️ ZnO(s) + C(s) → Zn(s) + CO(g)
⚗️ MnO₂ + 4HCl → MnCl₂ + 2H₂O + Cl₂
⚗️ Ca(OH)₂(aq) + CO₂(g) → CaCO₃(s) + H₂O(l)
🎉 Story का अंत — और एक ज़रूरी सीख
Class खत्म होने वाली थी। Sir ने चारों दोस्तों को देखा।
Arjun सोच रहा था — ‘तो जब मेरी cycle पर जंग लगेगी, वो displacement नहीं corrosion है!’
Priya मुस्कुरा रही थी — ‘Photography में decomposition… wow!’
Rohan notebook बंद करते हुए बोला — ‘Balancing equations practice करनी होगी।’
Sonu ने हाथ उठाया — ‘Sir, एक last question!’
💬 Sonu:
“Sir, क्या हमारे शरीर में भी chemical reactions होती हैं?”
💬 Sir Om Sikarwar:
“बिल्कुल Sonu! तुम्हारा हर साँस — Exothermic reaction।”
“तुम्हारा खाना पचना — Combination और Decomposition।”
“तुम्हारे muscles की energy — Glucose का oxidation।”
“यानी — तुम खुद एक चलती-फिरती Chemical Laboratory हो!”
🏆 BOARD EXAM TIPS — Teacher Om Sikarwar की तरफ से:
✅ हर reaction को उसके TYPE के साथ पहचानो
✅ Balanced equations में coefficients याद रखो
✅ Physical states (s), (l), (g), (aq) ज़रूर लिखो
✅ Exothermic vs Endothermic clearly explain करो
✅ Oxidising agent vs Reducing agent की definition याद रखो
✅ Corrosion और Rancidity के practical examples दो
NEET/IIT-JEE के लिए:
✅ Reactivity series की order याद रखो
✅ Electrolysis of water में cathode/anode clearly mention करो
✅ Photolytic decomposition को light-sensitive reactions से connect करो
Chemical Reactions and Equations Book Exercise
Exercise Answers — Simple & Easy Style
❓ Q3. What happens when dilute HCl is added to iron filings?
✅ Answer:
Answer: (d) Iron salt and water are produced.
💡 Jab HCl iron ke saath milta hai, iron chloride (salt) aur hydrogen gas banta hai. Option (d) sahi hai!
Q4. What is a balanced chemical equation? Why should it be balanced?
✅ Answer:
A balanced chemical equation is one where the number of atoms of each element is equal on both sides — reactants and products.
Equations must be balanced because of the Law of Conservation of Mass: atoms are never created or destroyed in a chemical reaction. So both sides must be equal!
💡 Yaad karo: Jo atoms andar jaate hain, wahi bahar aate hain — nature ka rule hai!
Q5. Translate into chemical equations and balance them:
✅ Answer:
(a) Hydrogen + Nitrogen → Ammonia
3H2 + N2 –> 2NH3
(b) Hydrogen sulphide burns in air → Water + Sulphur dioxide
2H2S + 3O2 –> 2H2O + 2SO2
(c) Barium chloride + Aluminium sulphate → Aluminium chloride + Barium sulphate
3BaCl2 + Al2(SO4)3 –> 2AlCl3 + 3BaSO4
(d) Potassium + Water → Potassium hydroxide + Hydrogen
2K + 2H2O –> 2KOH + H2 (gas)
Q6. Balance the following chemical equations:
✅ Answer:
(a) HNO3 + Ca(OH)2 → Ca(NO3)2 + H2O
2HNO3 + Ca(OH)2 –> Ca(NO3)2 + 2H2O
(b) NaOH + H2SO4 → Na2SO4 + H2O
2NaOH + H2SO4 –> Na2SO4 + 2H2O
(c) NaCl + AgNO3 → AgCl + NaNO3
NaCl + AgNO3 –> AgCl + NaNO3 (Already balanced!)
(d) BaCl2 + H2SO4 → BaSO4 + HCl
BaCl2 + H2SO4 –> BaSO4 + 2HCl
Q7. Write balanced equations for the following:
✅ Answer:
(a) Calcium hydroxide + Carbon dioxide → Calcium carbonate + Water
Ca(OH)2 + CO2 –> CaCO3 + H2O
(b) Zinc + Silver nitrate → Zinc nitrate + Silver
Zn + 2AgNO3 –> Zn(NO3)2 + 2Ag
(c) Aluminium + Copper chloride → Aluminium chloride + Copper
2Al + 3CuCl2 –> 2AlCl3 + 3Cu
(d) Barium chloride + Potassium sulphate → Barium sulphate + Potassium chloride
BaCl2 + K2SO4 –> BaSO4 + 2KCl
Q8. Write balanced equations and identify the type of reaction:
✅ Answer:
(a) KBr(aq) + BaI2(aq) → KI(aq) + BaBr2(s)
2KBr + BaI2 –> 2KI + BaBr2
Type: Double Displacement Reaction
(b) ZnCO3(s) → ZnO(s) + CO2(g)
ZnCO3 –> ZnO + CO2 (Already balanced!)
Type: Decomposition Reaction
(c) H2(g) + Cl2(g) → 2HCl(g)
H2 + Cl2 –> 2HCl (Already balanced!)
Type: Combination Reaction
(d) Mg(s) + HCl(aq) → MgCl2(aq) + H2(g)
Mg + 2HCl –> MgCl2 + H2
Type: Displacement Reaction
Q9. What are exothermic and endothermic reactions? Give examples.
✅ Answer:
Exothermic Reaction — heat is released (energy bahar aati hai).
Example: Burning of coal: C + O2 –> CO2 + Heat
C + O2 –> CO2 + Heat (Energy)
Endothermic Reaction — heat is absorbed (energy andar jaati hai).
Example: Photosynthesis — plants absorb sunlight to make food.
6CO2 + 6H2O + Sunlight –> C6H12O6 + 6O2
Q10. Why is respiration considered an exothermic reaction?
✅ Answer:
In respiration, glucose is broken down with oxygen to produce energy. Since energy (heat) is released, it is an exothermic reaction.
C6H12O6 + 6O2 –> 6CO2 + 6H2O + Energy
💡 Yeh energy hi hamein kaam karne aur garam rehne mein help karti hai!
Q11. Why are decomposition reactions called the opposite of combination reactions?
✅ Answer:
In a combination reaction, two or more substances join to form one new compound:
A + B –> AB
In a decomposition reaction, one compound breaks into simpler substances:
AB –> A + B
💡 Dono bilkul ulte hain — ek jodata hai, doosra todta hai!
Q12. Write one equation each for decomposition reactions (heat, light, electricity):
✅ Answer:
By Heat (Thermal Decomposition):
2Pb(NO3)2 –[Heat]–> 2PbO + 4NO2 + O2
By Light (Photodecomposition):
2AgCl –[Sunlight]–> 2Ag + Cl2
By Electricity (Electrolytic Decomposition):
2H2O –[Electricity]–> 2H2 + O2
Q13. Difference between displacement and double displacement reactions:
✅ Answer:
|
Feature |
Displacement |
Double Displacement |
|
What happens? |
One element replaces another |
Both elements swap with each other |
|
Example |
Zn + CuSO4 –> ZnSO4 + Cu |
NaCl + AgNO3 –> AgCl + NaNO3 |
Q14. Refining of silver — displacement reaction:
✅ Answer:
In the refining of silver, copper metal displaces silver from silver nitrate solution:
Cu + 2AgNO3 –> Cu(NO3)2 + 2Ag (precipitate)
💡 Copper, silver ko hataa deta hai — aur silver neeche settle ho jaata hai!
Q15. What is a precipitation reaction? Give examples.
✅ Answer:
When two solutions are mixed and an insoluble solid (precipitate) is formed, it is called a precipitation reaction.
Na2SO4 + BaCl2 –> BaSO4 (white ppt) + 2NaCl
💡 BaSO4 paani mein nahi ghulta — seedha neeche baith jaata hai!
Q16. Explain oxidation & reduction in terms of gain/loss of oxygen:
✅ Answer:
(a) Oxidation — gain of oxygen (or loss of hydrogen):
2Cu + O2 –> 2CuO (Copper gains oxygen – oxidised)
2Mg + O2 –> 2MgO
(b) Reduction — loss of oxygen (or gain of hydrogen):
CuO + H2 –> Cu + H2O (CuO loses oxygen – reduced)
Fe2O3 + 3CO –> 2Fe + 3CO2
Q17. Shiny brown element X turns black on heating. Name X and the black compound.
✅ Answer:
Element X = Copper (Cu)
Reaction:
2Cu + O2 –[Heat]–> 2CuO (black)
Black compound = Copper Oxide (CuO)
Q18. Why do we apply paint on iron articles?
✅ Answer:
Paint forms a protective layer that prevents oxygen and moisture from reaching the iron surface, thus stopping rusting (corrosion).
💡 Paint = shield for iron! Oxygen nahi pahunchti, rust nahi hoti.
Q19. Oil and fat containers are flushed with nitrogen. Why?
✅ Answer:
Nitrogen is an inert gas — it does not react with food. Oxygen would oxidise the fats/oils, causing rancidity (bad smell and taste). Nitrogen keeps the food fresh by displacing oxygen.
💡 Nitrogen = safe guardian of food! Oxygen ko bahar rakhta hai.
Q20. Explain Corrosion and Rancidity with examples:
✅ Answer:
(a) Corrosion — Slow destruction of metals by reacting with moisture/oxygen.
Example: Iron rusting when exposed to air and water:
4Fe + 3O2 + xH2O –> 2Fe2O3.xH2O (rust)
(b) Rancidity — Oxidation of fats and oils, causing bad smell/taste.
Example: Butter left open for days develops a bad smell — it has become rancid.
💡 Corrosion = metals kharaab hona | Rancidity = khana kharaab hona
classorb.com/chemical-reactions-equations-class-10-notes
— CLASS ORB.COM | Teacher: Om Sikarwar | Chapter 1 Complete —
