Some Basic Concepts of Chemistry-Chapter 1, Class 11 Easy Solution Notes
1. Chemistry kya hai?
बच्चों, सबसे पहले ये समझ लो – केमिस्ट्री क्या होती है!
सुबह जब तुम्हारी माँ चाय बनाती है… देगची में पानी, चाय पत्ती, दूध, चीनी डालती है और गरम करती है। थोड़ी देर बाद निकलती है चाय – बिलकुल अलग चीज़! चाय पत्ती घुल गया, दूध बदल गया, चीनी मिक्स हो गई, और पूरी चाय में नया रंग, महक और स्वाद आ गया। ये सब मिलकर एक नया पदार्थ बन गया – पहले वाले ingredients से completely different.
ये होता हैchemical change! मतलब पुराने चीज़ों को मिला के, गर्मी देके या react करके कुछ बिल्कुल नया बन जाता है। रसायन विज्ञान इसी का अध्ययन है: पदार्थ के बनने, बदलने और उसके गुणों का.
सिंपल है ना? अब अगर चाय को ठंडा करने के लिए fridge में डाल दो, तो सिर्फ state change होगा (physical change) – taste वही रहेगा.लेकिन अगर जला दी, तो नया compound बन जाएगा – वापस चाय नहीं बनेगी!
तो याद रखो: Chemistry विज्ञान में होने वाले परिवर्तन का विज्ञान, खास कर जब कुछ नया बन जाए जैसे कि मां की चाय!
Official definition किताब वाली :
रसायन विज्ञान वह विज्ञान की शाखा है जो पदार्थ के संगठन (composition), संरचना (structure), गुण (properties) और अभिक्रियाओं (reactions) का अध्ययन करती है.
लेकिन simple बोलूं तो – chemistry की चीजों की science और उनके बदलने की science! जो भी चीज दुनिया में है (फोन, पानी, हवा, खाना), उसकी बनावट, व्यवहार और बदलाव – – यही सब केमिस्ट्री है।
एक मज़ेदार बात: ये idea हमारे देश में बहुत पुराना है! लगभग 2600 साल पहले आचार्य कणाद (असली नाम कश्यप) ने कहा था कि सब पदार्थ छोटे-छोटे ‘अनु’ (tiny indivisible particles) से बने हैं. ये बिल्कुल modern atomic theory जैसा है!जब हम Dalton की theory पढ़ेंगे (1808), तब देखेंगे—कणाद जी ने 2500 साल पहले ही ये सोच ली थी। हमारा ancient science कितना advanced था!

Chemistry क्यों महत्वपूर्ण है? सोचो ज़रा –
जो दवाइयाँ लेते हो (बुखार, सर्दी, गंभीर बिमारी) – सब केमिस्ट्री से बनती हैं।
किसान जो खेत में खाद (fertiliser) डालता है – chemistry ही तो है।
Bike में petrol – जलकर energy देता है, pure chemical reaction!
पेट में खाना पहचानता है—enzymes और reactions से, ये भी chemistry!
सच में, chemistry har jagah hai – हर जगह है – घर से लेकर बॉडी तक। बिना इसके जिंदगी रुक जाती!
अब चलो आगे बढ़ते हैं. Matter क्या होता है?
ये short, clear aur engaging है –
2. Matter — क्या है, और उसकी तीन अवस्थाएँ
बच्चों, matter क्या होता है? बिल्कुल सरल: matter वह कुछ भी है जो mass रखता है और space (जगह) घेरता है।
उदाहरण से समझो – तुम्हारी book matter है (उसमें mass है, जगह लेती है), पानी matter है, हवा matter है (हाँ, हवा दिखती नहीं लेकिन उसका mass होता है और वह space भरती है)।
और यह petrichor की smell जो बारिश के बाद आती है (मिट्टी की खुशबू) – वह भी matter ही है! असल में soil के अंदर bacteria (actinomycetes) से geosmin नाम का molecule निकलता है। बारिश के पानी से वह उड़ जाता है और हमें smell आती है। ये सब molecules ही तो हैं – यानी matter!
अब matter की तीन physical states:
1. Solid (ठोस):
इसमें particles बहुत पास-पास और tight packed होते हैं। वे सिर्फ अपनी जगह पर vibrate कर सकते हैं, move नहीं कर सकते। इसलिए इनका shape और volume दोनों fixed होते हैं।
जैसे – ice, iron rod, या तुम्हारी table।
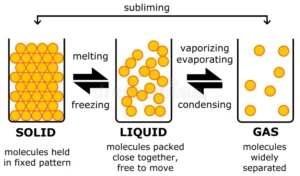
2. Liquid (द्रव):
इसमें particles पास होते हैं लेकिन एक-दूसरे के ऊपर slide कर सकते हैं और freely move करते हैं।
इसलिए volume fixed रहता है (ज़्यादा compress नहीं होता), लेकिन shape container के अनुसार बदल जाती है।
जैसे – पानी, दूध, oil – किसी भी container में डालो, उसी का shape ले लेते हैं।
3. Gas (गैस):
इसमें particles बहुत दूर-दूर होते हैं और तेज़ी से randomly move करते हैं।
इनका न shape fixed होता है, न volume – ये पूरा container भर लेते हैं।
जैसे – कमरे की हवा, LPG cylinder की gas (जब knob खोलते हैं तो फैल जाती है)।
याद रखने वाली बात:
ये तीनों states temperature और pressure से बदल सकती हैं –
जैसे ice को गरम करो तो पानी बन जाता है (melting), और पानी को गरम करो तो भाप (vaporization) बन जाती है।
निष्कर्ष:
सरल है ना? Matter हर जगह है, और उसकी states समझ गए तो chemistry की शुरुआत हो गई!
Physical vs Chemical Change
Physical change क्या होता है?
वह change जिसमें सिर्फ दिखाई देने वाली चीज़ें या state (अवस्था) बदलती है – लेकिन substance की असली identity वही रहती है।
मतलब substance वही रहता है, बस shape, size या form बदलता है।
🔹 Examples:
- Ice का पिघलकर पानी बनना – physical change। क्योंकि ice और पानी दोनों H₂O ही हैं! ठंडा करने पर फिर से ice बन जाता है – यानी reversible है।
- Paper को काटना या तोड़ना – physical। अभी भी paper ही है, बस छोटा हो गया।
- पानी का उबलना (steam बनना) या जमना – ये सब physical changes हैं।
Chemical change क्या होता है?
यह वह change है जिसमें बिल्कुल नया substance बन जाता है।
पुराना substance अपनी identity खो देता है और नए compounds बन जाते हैं।
यह आसानी से reverse नहीं होता।
Examples:
- Coal (कोयला) को जलाना – chemical change। Coal जलकर CO₂ gas और राख (ash) बन जाती है। वापस coal नहीं बन सकता!
- दूध से दही (curd) बनाना – chemical। Lactose को bacteria बदलकर lactic acid बना देते हैं, जिससे taste, smell और texture बदल जाता है।
- Iron में rust लगना – chemical। Iron + oxygen + moisture से Fe₂O₃ (rust) बनता है – वापस साफ iron आसानी से नहीं मिलता।
Exam tip (बहुत important – boards में आता है!)
अगर पूछा जाए कि यह chemical change है या नहीं, तो ये संकेत देखो:
- नया substance बन गया
- Colour बदल गया
- Gas निकल रही है (bubbles या smell)
- Smell बदल गई
- Heat निकली या absorb हुई
- आसानी से reverse नहीं हो सकता (irreversible)
याद रखने वाली बात:
- Physical change → substance वही रहता है (सिर्फ रूप बदलता है)
- Chemical change → substance ही बदल जाता है (नया बन जाता है)
निष्कर्ष:
अब clear हो गया?
अगली बार कोई change देखो तो सोचो:
क्या यह reversible है और substance वही है?
या नया substance बन गया?
(पदार्थ का वर्गीकरण)
अब बच्चों, हमने matter क्या है और उसके तीन states समझ लिए। तो अब ये समझते हैं कि matter को हम कैसे categorize करते हैं।
सबसे ऊपर level पर, सारी matter दो बड़े भागों में बंट जाती है:
- Pure Substance (शुद्ध पदार्थ)
- Mixture (मिश्रण)
चलो, एक-एक करके आसानी से समझते हैं।
Pure Substance (शुद्ध पदार्थ)
ये वो पदार्थ है जिसमें सिर्फ एक ही तरह के कण होते हैं। इसे और दो छोटे-छोटे भागों में बाँटा जाता है:
A. Elements (तत्व)
Element वो पदार्थ है जो सिर्फ एक ही प्रकार के atoms से बना होता है। इसे किसी भी chemical तरीके से और छोटा नहीं किया जा सकता।
उदाहरण:
- Gold (सोना) – पूरा सोने का टुकड़ा सिर्फ gold atoms से बना है।
- Iron (लोहा), Oxygen (ऑक्सीजन), Carbon (कार्बन), Hydrogen (हाइड्रोजन)।
आजकल दुनिया में कुल 118 elements खोजे गए हैं, और ये सब Periodic Table में रखे गए हैं।
B. Compounds (यौगिक)
Compound तब बनता है जब दो या दो से ज्यादा elements आपस में fixed ratio में chemically combine हो जाते हैं।
उदाहरण:
- Water (पानी) = H₂O मतलब हमेशा 2 hydrogen atoms + 1 oxygen atom। चाहे भारत में बने, अमेरिका में बने या चाँद पर बने – ratio कभी नहीं बदलता।
मजेदार बात ये है कि compound के गुण उसके elements से बिल्कुल अलग होते हैं।
जैसे:
- Hydrogen → जलता है (flammable gas)
- Oxygen → जलने में मदद करता है
- लेकिन दोनों मिलकर बने Water → आग बुझाता है!
देखा? नया पदार्थ बन गया, गुण भी पूरी तरह नए!
Mixture (मिश्रण)
Mixture में दो या ज्यादा पदार्थ मिले होते हैं, लेकिन chemically combine नहीं होते। यहाँ ratio fixed नहीं होता – जितना चाहो उतना मिला सकते हो।
उदाहरण:
- हवा (Air) – लगभग 78% nitrogen, 21% oxygen और बाकी थोड़े गैसें।
Mixture दो प्रकार के होते हैं:
- Homogeneous Mixture (समांगी मिश्रण) पूरे मिश्रण में हर जगह एक जैसा दिखता और लगता है। उदाहरण: नमक वाला पानी (salt water) – नमक पूरी तरह घुल जाता है, दिखता नहीं।
- Heterogeneous Mixture (विषमांगी मिश्रण) इसमें अलग-अलग भाग साफ दिखते हैं। उदाहरण:
- रेत और लोहे की बारीक filings
- सलाद (salad) – टमाटर, खीरा, पत्ता अलग-अलग दिखते हैं।
- पेंच नदी का पानी – इसमें minerals, मिट्टी के कण, छोटे जीवाणु सब मिले रहते हैं।
ध्यान रखो: पेंच नदी का पानी mixture है, शुद्ध पानी (H₂O) compound है। दोनों को confuse मत करना।
सबसे महत्वपूर्ण अंतर:
- Mixture के components को physical methods से अलग किया जा सकता है। जैसे: muddy water को filter कर सकते हो, salt water को evaporate करके नमक वापस ले सकते हो।
- लेकिन Compound को elements में अलग करने के लिए chemical reaction करनी पड़ती है। पानी को हाइड्रोजन और ऑक्सीजन में अलग करने के लिए electricity से electrolysis करना पड़ता है।
समझ आया बच्चों? Pure substance = सिर्फ एक तरह के atoms या fixed ratio में बने compounds Mixture = अलग-अलग चीजें बस मिली हुईं, ratio बदल सकता है।
4. SI Units — why measurements need units
Imagine someone tells you the answer is ‘5’. Five what? Five litres? Five kilograms? Five seconds? Without a unit, a number is meaningless. This is why scientists all over the world agreed on a common system called the SI system (Système International d’Unités).
There are 7 base units. For chemistry, the most important ones are:
|
Physical Quantity |
SI Unit |
Symbol |
|
Mass |
Kilogram |
kg |
|
Length |
Metre |
m |
|
Time |
Second |
s |
|
Temperature |
Kelvin |
K |
|
Amount of substance |
Mole |
mol |
|
Electric current |
Ampere |
A |
|
Luminous intensity |
Candela |
cd |
4. Mass और Weight में फर्क (बहुत Important!)
अरे बच्चों, एक चीज है जो लगभग हर student को confuse कर देती है – Mass और Weight। दोनों लगते तो एक जैसे हैं, लेकिन बिल्कुल अलग हैं। ध्यान से सुनो।
Mass क्या है? Mass मतलब किसी चीज में कितना matter है। ये quantity है, और ये कहीं भी नहीं बदलती। तुम्हारा mass यहाँ Indore में 50 kg है, तो चाँद पर भी 50 kg ही रहेगा, मंगल पर भी 50 kg ही रहेगा। Mass कभी नहीं बदलता।
Weight क्या है? Weight मतलब गुरुत्वाकर्षण (gravity) के कारण लगने वाला बल। Formula है: Weight = Mass × g (g = acceleration due to gravity)
पृथ्वी पर g ≈ 9.8 m/s² है, लेकिन चाँद पर g सिर्फ पृथ्वी का 1/6 है। इसलिए अगर तुम्हारा weight यहाँ 50 kg (actually 490 Newton) है, तो चाँद पर सिर्फ 8-9 kg जैसा feel होगा।
याद रखो: Chemistry और Physics में हम हमेशा Mass की बात करते हैं, Weight की नहीं। Weight जगह-जगह बदलता है, Mass नहीं बदलता।

Temperature – Celsius या Kelvin?
रोजमर्रा की जिंदगी में हम Celsius (°C) इस्तेमाल करते हैं। लेकिन chemistry और physics में ज्यादातर Kelvin (K) इस्तेमाल होता है।
Conversion बहुत आसान है: K = °C + 273
उदाहरण:
- 0°C = 273 K
- 25°C = 298 K
- 100°C = 373 K
अब सवाल ये है – Kelvin क्यों इस्तेमाल करते हैं? क्योंकि 0 K को Absolute Zero कहते हैं। यहाँ theoretically सारे molecules का motion रुक जाता है। 0 K से नीचे तापमान कभी नहीं जा सकता। इसलिए scientific calculations में Kelvin ज्यादा सही और useful है।
⚠ Exam Tip: Gas laws (जैसे Boyle’s law, Charles’ law) में temperature हमेशा Kelvin में ही लिखनी होती है। Celsius में लिखोगे तो answer गलत हो जाएगा!
5. Scientific Notation और Significant Figures
बच्चों, chemistry में बहुत बड़ी और बहुत छोटी संख्याएँ आती हैं। जैसे एक hydrogen atom का mass: 0.00000000000000000000000166 gram
इसे बार-बार लिखना मुश्किल है ना?
इसलिए हम Scientific Notation इस्तेमाल करते हैं।
Scientific Notation का Rule: कोई भी संख्या को हम इस रूप में लिखते हैं → N × 10ⁿ जहाँ 1 ≤ N < 10
उदाहरण:
- एक hydrogen atom का mass = 1.66 × 10⁻²⁴ g
- Avogadro’s number = 6.022 × 10²³
- 2500 = 2.5 × 10³
- 0.0038 = 3.8 × 10⁻³
- प्रकाश की गति = 3.0 × 10⁸ m/s
बहुत आसान तरीका याद रखो:
- बहुत बड़ी संख्या → घात (power) positive
- बहुत छोटी संख्या → घात negative
गुणा और भाग कैसे करें?
- गुणा: N वाले भाग को गुणा करो और powers को जोड़ दो
- भाग: N वाले भाग को भाग करो और powers को घटा दो
Practice करो बच्चों, ये पूरे साल calculations में बार-बार आएगा।
Significant figures — honestly, this confuses a lot of students
Significant figures (sig figs) tell us how precise a measurement is. When you measure something, you can only be as precise as your instrument allows. If you say a rod is 5 cm, that’s different from saying it’s 5.0 cm or 5.00 cm. Each of these implies a different level of precision.
The rules, and please learn these properly:
- All non-zero digits are significant. So 234 has 3 sig figs, 7.89 has 3 sig figs.
- Zeros between non-zero digits are significant. 205 has 3 sig figs. 10.07 has 4 sig figs.
- Leading zeros (before the first non-zero digit) are NOT significant. 0.0045 has only 2 sig figs.
- Trailing zeros after a decimal point are significant. 2.500 has 4 sig figs. 3.00 has 3 sig figs.
- Trailing zeros in a whole number — ambiguous. Better to write in scientific notation. 2500 could be 2, 3, or 4 sig figs. Write 2.5 × 10³ for 2 sig figs, or 2.500 × 10³ for 4 sig figs.
For calculations: in multiplication/division, the answer should have as many sig figs as the measurement with the fewest sig figs. In addition/subtraction, round off based on decimal places (not sig figs). This comes in calculations, so pay attention to it.
6. Laws of Chemical Combination (रासायनिक संयोग के नियम)
अब बच्चों, असली मज़ा शुरू होता है!
जॉन डाल्टन ने अपनी Atomic Theory देने से पहले भी वैज्ञानिकों ने बहुत सारे प्रयोग किए थे। उन प्रयोगों से कुछ खास पैटर्न निकले, जिन्हें हम Laws of Chemical Combination कहते हैं।
ये नियम chemistry की नींव हैं। इन्हें अच्छे से समझ लो, क्योंकि आगे सारी calculations इन्हीं पर आधारित हैं।
ये मुख्य रूप से पाँच नियम हैं:
1. Law of Conservation of Mass
(द्रव्यमान संरक्षण का नियम)
Joseph Proust और Antoine Lavoisier ने यह नियम दिया।
क्या कहता है? “किसी भी रासायनिक अभिक्रिया में, कुल द्रव्यमान पहले और बाद में बराबर रहता है। Matter न तो बनता है, न नष्ट होता है – सिर्फ रूप बदलता है।”
सरल उदाहरण: जब तुम लोहे की कील को जंग लगाते हो (iron + oxygen → rust), तो जंग का वजन लोहे + ऑक्सीजन के कुल वजन के बराबर ही होता है। कुछ भी गायब नहीं होता!
याद रखने वाली बात: ये नियम बताता है – chemistry में mass हमेशा conserved रहता है।
2. Law of Definite Proportions (Constant Proportions)
(निश्चित अनुपात का नियम)
Joseph Proust द्वारा दिया गया।
क्या कहता है? “कोई भी compound हमेशा fixed ratio (निश्चित अनुपात) में elements से बना होता है। ये ratio mass के हिसाब से हमेशा वही रहता है, चाहे compound कहीं से भी लिया जाए।”
उदाहरण: पानी (H₂O) हमेशा 2 भाग hydrogen और 16 भाग oxygen (1:8 ratio) से बनता है। चाहे नदी का पानी हो, बारिश का पानी हो या बोतल का पानी – ratio कभी नहीं बदलता।
3. Law of Multiple Proportions
(बहुल अनुपात का नियम)
John Dalton ने यह नियम दिया।
क्या कहता है? “जब दो elements एक से ज्यादा compounds बनाते हैं, तो एक element का fixed mass दूसरे element के mass के साथ simple whole number ratio में होता है।”
उदाहरण: Carbon और Oxygen दो compounds बनाते हैं:
- Carbon monoxide (CO) → 12g carbon + 16g oxygen
- Carbon dioxide (CO₂) → 12g carbon + 32g oxygen
यहाँ oxygen का mass 16 : 32 = 1 : 2 ratio है – जो simple whole number है।
4. Law of Reciprocal Proportions (or Law of Equivalent Proportions)
(व्युत्क्रम अनुपात का नियम)
Richter द्वारा दिया गया।
क्या कहता है? “अगर दो elements A और B अलग-अलग एक third element C से combine होते हैं, तो A और B का आपस में भी वही अनुपात होगा जिसमें वे C के साथ combine होते हैं।”
(ये थोड़ा tricky है, इसलिए आगे जब examples करेंगे तब और अच्छे से समझाएंगे)
5. Gay-Lussac’s Law of Gaseous Volumes
(गैसीय आयतनों का नियम)
Joseph Louis Gay-Lussac द्वारा दिया गया।
क्या कहता है? “गैसों की रासायनिक अभिक्रिया में, reactants और products के आयतन (volume) simple whole number ratio में होते हैं। (जब तापमान और दबाव constant हो)”
उदाहरण: हाइड्रोजन + ऑक्सीजन → पानी 2 volume H₂ + 1 volume O₂ → 2 volume water vapour Ratio = 2 : 1 : 2
समाप्ति में:
बच्चों, ये पाँचों नियम chemistry की नींव हैं। इन्हें याद रखो और समझ लो, क्योंकि जब हम Dalton की Atomic Theory पढ़ेंगे, तब ये सारे नियम एकदम clear हो जाएंगे कि डाल्टन ने इन्हीं नियमों को देखकर atomic theory बनाई थी।
7. Dalton’s Atomic Theory (डाल्टन का परमाणु सिद्धांत)
अब बच्चों, आ गया वो सबसे महत्वपूर्ण टॉपिक!
1808 में एक अंग्रेज़ chemist और स्कूल टीचर John Dalton ने अपनी Atomic Theory प्रकाशित की। उस समय ये theory इतनी बड़ी बात थी कि सारी chemistry की दुनिया बदल गई।
ये theory हमने अभी जो पाँच Laws of Chemical Combination पढ़े थे – उन सबको एक साथ explain कर देती थी।
Dalton के मुख्य Postulates (मुख्य बातें)
डाल्टन ने पाँच मुख्य बातें बताईं:
- Matter बहुत छोटे-छोटे, indivisible कणों से बना है, जिन्हें हम Atom कहते हैं। (परमाणु को और नहीं काटा जा सकता)
- एक ही element के सारे atoms एक जैसे होते हैं – mass और chemical properties दोनों में। (सारे सोने के परमाणु बिल्कुल एक जैसे)
- दूसरे element के atoms का mass और properties अलग होते हैं।
- Atoms साधारण पूर्ण संख्या (simple whole number) के अनुपात में मिलकर compounds बनाते हैं। जैसे H₂O में 2 hydrogen + 1 oxygen।
- रासायनिक अभिक्रिया में atoms न तो बनते हैं, न नष्ट होते हैं – सिर्फ rearrange (एक जगह से दूसरी जगह लगते) हैं।
इसी वजह से Law of Conservation of Mass और Law of Definite Proportions समझ में आ जाते थे।
अब Limitations (कमियाँ) – ये exam में जरूर पूछते हैं
डाल्टन की theory बहुत अच्छी थी, लेकिन पूरी सही नहीं थी। बाद में कुछ कमियाँ निकलीं:
- Atoms divisible हैं आज हम जानते हैं कि atom के अंदर electron, proton और neutron होते हैं। Atom को तोड़ा जा सकता है।
- एक ही element के सारे atoms बिल्कुल एक जैसे नहीं होते Isotopes होते हैं – same element, लेकिन mass अलग। जैसे Carbon-12 और Carbon-14।
- सभी compounds simple whole number ratio में नहीं बनते कुछ non-stoichiometric compounds होते हैं, जिनमें ratio साधारण संख्या नहीं होती।
भारतीय कनेक्शन – आचार्य कणाद
बच्चों, एक रोचक बात! हमारे देश में लगभग 2600 साल पहले (600 BCE) आचार्य कणाद (कश्यप) ने कहा था कि सारा matter छोटे-छोटे indivisible कणों से बना है, जिन्हें उन्होंने ‘परमाणु’ नाम दिया। ‘परमाणु’ शब्द का मतलब ही है – “जिसे और काटा न जा सके”।
डाल्टन ने इसे scientific experiments के आधार पर प्रस्तुत किया, लेकिन विचार तो हमारे प्राचीन भारतीय ऋषियों ने बहुत पहले सोच लिया था!
अंत में…
हालाँकि Dalton की theory में कुछ limitations हैं, लेकिन आज भी ये theory बहुत useful है। खासकर ये बात आज भी 100% सही है कि: “Chemical reaction में atoms सिर्फ rearrange होते हैं – बनते या नष्ट नहीं होते।”
ये concept आज भी पूरी modern chemistry की नींव है।
समाप्ति:
तो बच्चों, Dalton की Atomic Theory को अच्छे से समझ लो। ये theory chemistry का आधार है।
8. Atomic Mass और Molecular Mass
बच्चों, अब एक बहुत जरूरी चीज समझते हैं।
परमाणु इतने छोटे होते हैं कि उन्हें तराजू पर नहीं तौला जा सकता। एक कार्बन परमाणु का mass सिर्फ 1.993 × 10⁻²³ gram है। हर बार इतनी छोटी संख्या लिखना या गिनना बहुत मुश्किल है ना?
इसलिए वैज्ञानिकों ने एक बहुत होशियार तरीका निकाला – Relative Atomic Mass।
Atomic Mass क्या है?
उन्होंने Carbon-12 को स्टैंडर्ड मान लिया और उसका atomic mass ठीक 12 रख दिया। फिर बाकी सभी elements का atomic mass, Carbon-12 के हिसाब से relative (तुलनात्मक) निकाला।
उदाहरण:
- Hydrogen का atomic mass ≈ 1
- Oxygen का ≈ 16
- Iron का ≈ 56
- Sodium का ≈ 23
- Chlorine का ≈ 35.5
Unit: इसे ‘u’ (unified mass unit) या amu कहते हैं। 1 u = Carbon-12 परमाणु के mass का ठीक 1/12वाँ भाग (1 u = 1.66 × 10⁻²⁴ gram) – ये value सिर्फ समझने के लिए, याद करने की जरूरत नहीं।
Molecular Mass क्या है?
Molecular mass = एक molecule में मौजूद सभी atoms के atomic masses का योग (sum)
बहुत आसान है, बस atoms को सही से गिनना है।
उदाहरण:
- Water (H₂O) = 2 × 1 + 16 = 18 u
- Carbon dioxide (CO₂) = 12 + 2 × 16 = 44 u
- Sulphuric acid (H₂SO₄) = 2(1) + 32 + 4(16) = 2 + 32 + 64 = 98 u
- Glucose (C₆H₁₂O₆) = 6×12 + 12×1 + 6×16 = 72 + 12 + 96 = 180 u
Ionic Compounds में क्या कहते हैं?
NaCl, MgO, CaCO₃ जैसे ionic compounds में “molecule” नहीं होता। इसलिए इन्हें Formula Mass कहते हैं।
उदाहरण: NaCl का formula mass = 23 + 35.5 = 58.5 u
बाकी calculation बिल्कुल same है, सिर्फ नाम formula mass हो जाता है।
⚠ Exam Tip (बहुत महत्वपूर्ण)
नीचे दिए atomic masses को अच्छे से याद कर लो। ये हर numerical में काम आएंगे:
- H = 1
- C = 12
- N = 14
- O = 16
- Na = 23
- S = 32
- Cl = 35.5
- Fe = 56
- Cu = 63.5
ये values बार-बार इस्तेमाल होंगी, इसलिए memorise कर लो।
Note:
तो बच्चों, आज हमने सीखा कि परमाणु का mass कैसे मापा जाता है और molecule का mass कैसे निकाला जाता है। बहुत simple है – बस Carbon-12 को 12 मानकर बाकी सब relative mass निकालते हैं।
9. Mole Concept — Chemistry का दिल
बच्चों, अब आ गया वो सबसे महत्वपूर्ण और सबसे powerful concept – Mole Concept। ये chemistry के सारे numericals का आधार है। एक बार ये समझ आ गया, तो सारी calculations बहुत आसान हो जाती हैं। चलो step by step, बिल्कुल सरल भाषा में समझते हैं।
रोजमर्रा की जिंदगी से समझो
हम रोज चीजें गिनते हैं तो छोटे-छोटे groups बना लेते हैं क्योंकि एक-एक करके गिनना मुश्किल होता है। जैसे:
- अंडे dozen में आते हैं (12)
- चूड़ियाँ gross में आती हैं (144)
- पेंसिलें box में 12 या 24
ठीक उसी तरह atoms और molecules इतने छोटे होते हैं कि उन्हें एक-एक करके नहीं गिना जा सकता। इसलिए वैज्ञानिकों ने एक बहुत बड़ा group बनाया जिसका नाम है Mole।
1 mole = 6.022 × 10²³ particles इसे Avogadro’s number या Avogadro’s constant (Nₐ) कहते हैं।
मतलब:
- 1 mole water molecules = 6.022 × 10²³ पानी के molecules
- 1 mole iron atoms = 6.022 × 10²³ लोहे के atoms
- 1 mole electrons = 6.022 × 10²³ electrons
Molar Mass क्या है?
Molar mass = एक mole substance का mass, gram में (g/mol)
सबसे खास बात: जो molecular mass या formula mass हम u (unified mass unit) में निकालते हैं, वही संख्या gram में molar mass हो जाती है।
उदाहरण:
- Water का molecular mass = 18 u → इसलिए molar mass = 18 g/mol मतलब 18 gram पानी में ठीक 6.022 × 10²³ पानी के molecules होते हैं।
- Carbon का atomic mass = 12 u → molar mass = 12 g/mol 12 gram carbon में 6.022 × 10²³ carbon atoms
- Iron का atomic mass = 56 u → molar mass = 56 g/mol 56 gram iron में 6.022 × 10²³ iron atoms
देखा? अलग-अलग mass, लेकिन atoms की संख्या एक ही!
Avogadro’s number कितना बड़ा है?
कल्पना करो – अगर 1 mole चावल के दाने (rice grains) हो तो वो सारी पृथ्वी की सतह को कई किलोमीटर ऊँचाई तक ढक देंगे! और ये सिर्फ 18 gram पानी में होते हैं। सोचो कितने छोटे हैं atoms!
तीन मुख्य Mole Relationships (हर numerical में ये तीन काम आते हैं)
- Number of moles (n) = Given mass (w) ÷ Molar mass (M) n = w / M
- Number of particles = n × Nₐ = n × 6.022 × 10²³
- Gases के लिए (STP पर): 1 mole gas = 22.4 litre volume (Molar volume)
Example (बच्चों, ध्यान से देखो)
Question: 9 gram पानी में कितने molecules हैं?
Solution:
- Molar mass of H₂O = 18 g/mol
- n = 9 / 18 = 0.5 mol
- Molecules = 0.5 × 6.022 × 10²³ = 3.011 × 10²³ molecules
बस इतना simple!
Exam Tip (बहुत जरूरी)
हर numerical में पहला step हमेशा moles निकालो। Moles ही bridge है। Moles निकाल लिया तो particles, volume, mass – कुछ भी पूछो, आसानी से निकाल सकते हो।
तो बच्चों, आज हमने chemistry का सबसे महत्वपूर्ण concept समझ लिया – Mole Concept। ये समझ आ गया तो बाकी सारा numerical chemistry मजेदार लगेगा।
10. Stoichiometry — रासायनिक अभिक्रियाओं का हिसाब-किताब
बच्चों, अब आ गया chemistry का असली mathematical part – Stoichiometry।
शब्द ग्रीक भाषा से आया है – “Stoicheion” मतलब तत्व और “Metron” मतलब माप। सरल भाषा में कहें तो – रासायनिक अभिक्रिया में कितना reactant लगेगा और कितना product बनेगा, इसका हिसाब।
Balanced Chemical Equation ही सब कुछ बताता है
सबसे पहले equation को balance करना जरूरी है।
उदाहरण लो एक famous reaction का:
N₂ + 3H₂ → 2NH₃
ये equation हमें क्या बताता है?
- 1 mole nitrogen (N₂) reacts with 3 moles hydrogen (H₂)
- और बनता है 2 moles ammonia (NH₃)
Mass के रूप में भी देख लो:
- 28 g N₂ + 6 g H₂ → 34 g NH₃ (28 + 6 = 34 → द्रव्यमान संरक्षण का नियम सही!)
Stoichiometry Problem कैसे Solve करते हैं?
हर stoichiometry के numerical में यही तरीका इस्तेमाल होता है:
- Equation को balance करो
- Given mass को moles में बदलो
- Balanced equation से mole ratio निकालो
- फिर moles को वापस mass या जो unit पूछा हो उसमें बदल दो
Limiting Reagent (सीमित अभिकर्मक) – बहुत Important!
ये concept रोजमर्रा की जिंदगी से बहुत आसानी से समझ आता है।
कल्पना करो तुम 10 लोगों के लिए चाय बना रहे हो।
- दूध तो 20 कप के लिए काफी है
- लेकिन चाय पत्ती सिर्फ 8 कप के लिए है
तो तुम सिर्फ 8 कप चाय बना पाओगे। क्योंकि चाय पत्ती खत्म हो जाएगी पहले। यहाँ चाय पत्ती तुम्हारा limiting reagent है।
Chemistry में Limiting Reagent वो reactant होता है जो reaction में सबसे पहले पूरी तरह consume (खत्म) हो जाता है। वही decide करता है कि कितना product बनेगा। बाकी reactant excess (अधिक) में होता है, कुछ बच जाता है।
Limiting Reagent कैसे निकालें? (Step-by-step)
- दोनों reactants की given mass को moles में बदलें।
- हर reactant के moles को उसके balanced equation वाले coefficient से भाग दो।
- जिसका नंबर सबसे छोटा है, वही limiting reagent है।
Product की मात्रा हमेशा limiting reagent से ही calculate करनी चाहिए, excess वाले से नहीं।
Percentage Yield
असली प्रयोगशाला में हम जो product चाहते हैं, वो हमेशा 100% नहीं मिलता। कुछ product खराब हो जाता है, कुछ side reaction हो जाती है।
Percentage Yield = (Actual yield / Theoretical yield) × 100
(Actual yield = जो मिला Theoretical yield = limiting reagent से calculate किया गया maximum possible yield)
Exam Tip (बहुत जरूरी)
हर stoichiometry problem में याद रखो:
- सबसे पहले equation को balance करो
- सबको moles में बदलो
- Mole ratio से calculate करो
- अगर दो reactants की मात्रा दी हो तो हमेशा limiting reagent चेक करो
ये तीन स्टेप्स अगर ठीक से कर लोगे तो 90% numerical सही हो जाएंगे!
Quick Revision — Exam से पहले ये मत भूलना! (सबसे Important Points)
बच्चों, परीक्षा से पहले इस पेज को कम से कम दो बार जरूर पढ़ लो। ये सारे मुख्य points हैं जो बार-बार पूछे जाते हैं।
Basic Concepts
- Chemistry क्या है? → पदार्थ का अध्ययन (matter की बनावट, गुण और परिवर्तन)।
- Matter → जिसका mass हो और जो जगह घेरता हो।
- तीन अवस्थाएँ: Solid, Liquid, Gas।
- Physical Change: नया पदार्थ नहीं बनता (जैसे पानी का बर्फ बनना)।
- Chemical Change: नया पदार्थ बनता है (जैसे चाय बनाना)।
Classification of Matter
- Element: सिर्फ एक प्रकार के atoms (जैसे Gold, Oxygen)।
- Compound: दो या ज्यादा elements fixed ratio में (जैसे H₂O)।
- Mixture: variable ratio, physically मिले हुए (जैसे हवा, नमक पानी)।
Mass vs Weight
- Mass: हर जगह समान रहता है (constant)।
- Weight: gravity पर depend करता है, जगह बदलने पर बदलता है।
- Kelvin: °C + 273। 0 K = Absolute Zero (सबसे कम तापमान)।
Scientific Notation
- संख्या को लिखने का छोटा रूप: N × 10ⁿ (जहाँ 1 ≤ N < 10)।
Laws of Chemical Combination (5 मुख्य नियम)
- Conservation of Mass (द्रव्यमान संरक्षण)
- Definite Proportions (निश्चित अनुपात)
- Multiple Proportions (बहुल अनुपात)
- Gay-Lussac’s Law of Gaseous Volumes
- Avogadro’s Law (आवोगाद्रो का यम)
Dalton’s Atomic Theory
- Matter छोटे indivisible atoms से बना है।
- एक element के सभी atoms एक जैसे होते हैं।
- Atoms rearrange होते हैं, बनते या नष्ट नहीं होते।
- Limitations: Atoms divisible हैं, Isotopes होते हैं।
Atomic & Molecular Mass
- Atomic mass → Carbon-12 के आधार पर relative।
- 1 u = 1.66 × 10⁻²⁴ g।
- Molar mass (g/mol) = Molecular mass (u) में संख्या बराबर।
Mole Concept (सबसे महत्वपूर्ण)
- 1 Mole = 6.022 × 10²³ particles (Avogadro’s number)।
- n = Mass / Molar mass
- Number of particles = n × 6.022 × 10²³
- STP पर 1 mole gas = 22.4 litre
Stoichiometry & Limiting Reagent
- Balanced equation से mole ratio निकालकर calculations करते हैं।
- Limiting Reagent: वो reactant जो पहले खत्म हो जाए, product की मात्रा उसी से तय होती है।
- Excess reagent बच जाता है।
Exam Tip: ये सारे points याद रखो। खासकर:
- Mole formulas
- Limiting reagent कैसे निकालते हैं
- Dalton की limitations
- Mass vs Weight
- Kelvin conversion
ये revision sheet तुम्हारे पास हमेशा रखो। रात को सोने से पहले और सुबह उठकर एक बार पढ़ लो – सारे concepts तरोताजा हो जाएंगे!
Some Basic Concepts of Chemistry-Chapter 1, Class 11 Easy Solution NotesChemistry_Ch1_QuestionBank_NEET_JEEhh
Some Basic Concepts of Chemistry-Chapter 1, Class 11 Easy Solution Notes
